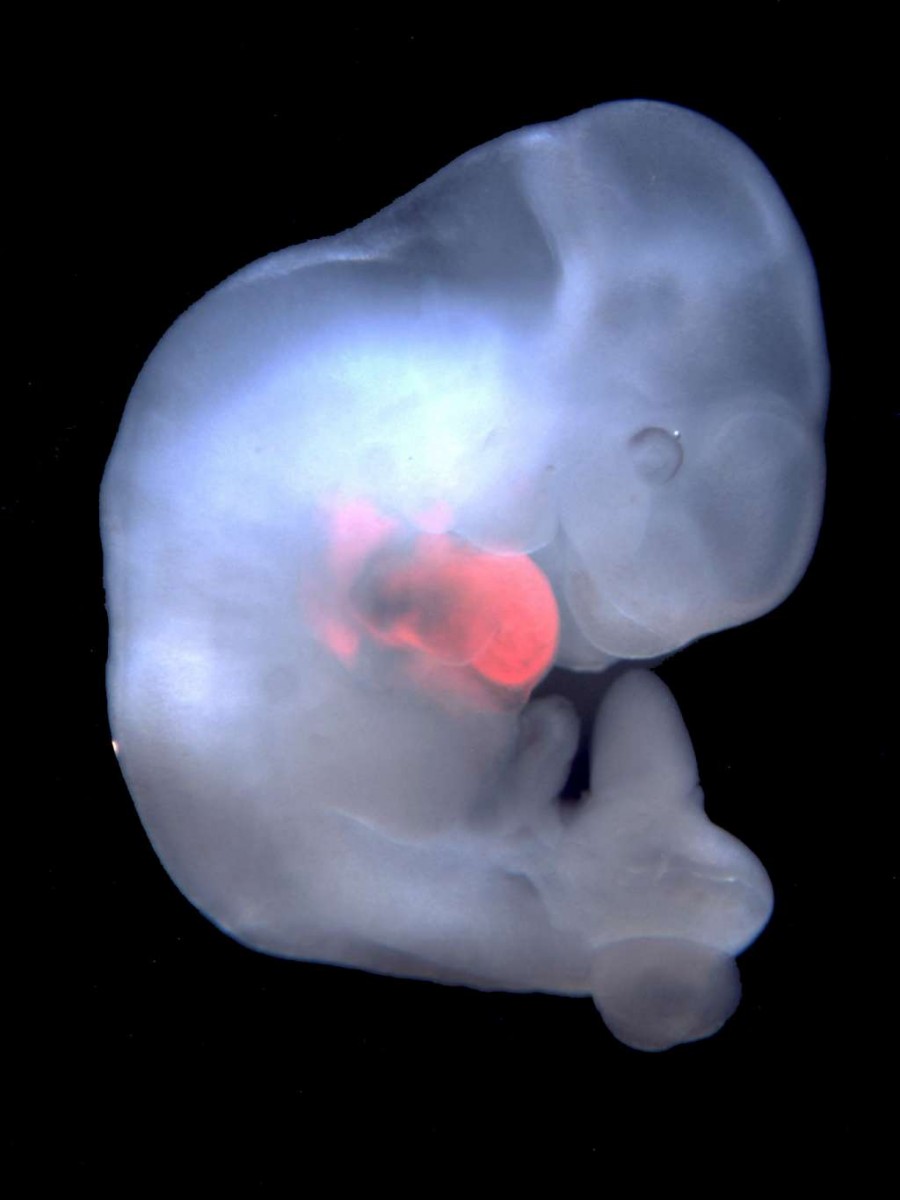
Wetenschappers zoeken op dit moment uit of het werkt en stoppen daartoe menselijke stamcellen in de embryo’s van dieren.
Het resultaat is een chimeer, oftewel twee dieren afkomstig uit verschillende bevruchtte eicellen. Vorig jaar stopten onderzoekers menselijke stamcellen in de embryo’s van varkens en runderen. En nu krijgt dat toen al veelbesproken onderzoek een vervolg. Tijdens een bijeenkomst van de American Association of Science kondigde dezelfde onderzoeksgroep aan nu ook menselijke stamcellen in embryo’s van schapen te hebben gestopt.
Donororganen
Het lijken misschien krankzinnige experimenten, maar de onderzoekers hebben een helder doel voor ogen, zo vertelt ontwikkelingsbioloog Bernard Roelen aan Scientias.nl. “De gedachte is dat je een varkensembryo maakt, waarbij het embryo zo is aangepast dat het bijvoorbeeld geen alvleesklier ontwikkelt. Vervolgens breng je menselijke stamcellen in met als doel een menselijke alvleesklier in dat varken te maken.” Als die alvleesklier ‘af’ is, zouden we deze uit het varken kunnen halen en in een mens kunnen transplanteren. Het zou – in theorie – een geweldige oplossing zijn voor het grote tekort aan donororganen. Bovendien zou door het gebruik van patiëntspecifieke stamcellen de kans op afstoting van het donororgaan enorm verkleind kunnen worden.

Fractie
Het klinkt te mooi om waar te zijn. Maar Amerikaanse onderzoekers zien blijkbaar genoeg mogelijkheden om het idee in ieder geval voorzichtig te verkennen. Eerst met behulp van runder- en varkensembryo’s en nu ook met schapenembryo’s. Tijdens beide onderzoeken bestond maar een fractie van de embryo’s uit menselijke cellen: in de studie uit 2017 was ongeveer 1 op de 100.000 cellen in de embryo’s afkomstig van mensen. In het recente onderzoek zou het naar verluidt gaan om 1 op de 10.000 cellen.
Wat doen die stamcellen?
Veel interessanter dan de oorspronkelijke verhouding tussen de menselijke en dierlijke cellen is natuurlijk de vraag wat die menselijke stamcellen in zo’n embryo gaan doen. Of, in de woorden van Roelen: “Kunnen ze een bijdrage leveren aan de vorming van een ander organisme?” Eerdere experimenten met ratten en muizen waren wat dat betreft hoopgevend. “Onderzoekers brachten pluripotente stamcellen (zie kader, red.) van muizen in een embryo van een rat en creëerden zo een rat met een muizen-alvleesklier. En omgekeerd lukte het ook: men kon dus ook een muis met een ratten-alvleesklier maken. Maar daarbij moet worden opgemerkt dat muizen en ratten redelijk op elkaar lijken.” Heel anders is dat met mensen, varkens en schapen. En dat blijkt ook wel uit de experimenten van vorig jaar. “Ze waren eigenlijk een beetje teleurstellend. Zo bleken de menselijke cellen in het varken niet veel te doen. In de runder-embryo’s wisten de menselijke cellen iets beter in leven te blijven. Maar een rund is een groot dier en je kunt je afvragen of het praktisch is om in zo’n dier menselijke organen te kweken.”
Tot het kweken van organen kwam het in de aangehaalde studies nooit. Zowel in het onderzoek met de varkens en runderen als in het onderzoek met de schapen werden de embryo’s in een draagmoeder geplaatst, alwaar de foetussen zich hooguit enkele weken mochten ontwikkelen alvorens gedood te worden. Hoewel de experimenten maar van korte duur waren, kunnen ze een schat aan informatie opleveren. “In die eerste weken is de aanleg van de organen al begonnen en kun je dus al zien of de menselijke stamcellen daar een rol in hebben gespeeld.” Dat de experimenten – die in Nederland strikt verboden zijn – maar kort liepen, heeft ongetwijfeld te maken met het feit dat de onderzoekers zich op onbekend terrein begeven. Niemand weet wat menselijke stamcellen precies gaan doen als je ze in een dierlijk embryo stopt. Want wij kunnen ze wel ‘programmeren’ om een alvleesklier te maken, maar misschien gaan ze ook nog wel andere dingen doen. “Dat moet je eigenlijk kunnen controleren, want je wilt natuurlijk niet een varken gaan maken met menselijke hersenen of een menselijke huid of – als het van het vrouwelijk geslacht is – een varken dat menselijke eicellen kan gaan produceren.” En zolang we geen goed beeld hebben van de impact die onze stamcellen op een embryo van een andere soort heeft, is voorzichtigheid geboden. “Vandaar dat men er ook voor kiest om de dieren niet geboren te laten worden.”
Grootste uitdaging
Het moge duidelijk zijn dat het onderzoek naar het kweken van menselijke organen in andere soorten nog in de kinderschoenen staat. Er zijn dan ook nog heel wat hobbels te nemen. “De grootste uitdaging is dat we op dit moment niet weten in hoeverre menselijke stamcellen in een dierlijke foetus een bijdrage kunnen leveren aan de vorming van weefsel. Wij staan genetisch gezien zo ver af van het varken of het schaap dat er misschien wel helemaal geen communicatie mogelijk is tussen hun en onze cellen.” En daarmee zou een samenwerking tussen die cellen – nodig voor de totstandkoming van complexe organen zoals een alvleesklier – onmogelijk zijn. Maar ook als het wél lukt om menselijke organen te kweken in bijvoorbeeld een varken zullen we voor nieuwe uitdagingen komen te staan. “Zo’n orgaan zal helemaal uit menselijke cellen bestaan,” aldus Roelen. “Maar de bloedvaten in het orgaan zullen deels bestaan uit cellen van het varken. En daar moeten we dan nog wel iets op bedenken, want die varkenscellen worden door ons immuunsysteem als lichaamsvreemd beschouwd en dus afgestoten.”
Ethische bezwaren
Maar het kweken van menselijke organen in andere diersoorten wordt niet alleen getergd door praktische uitdagingen. Er zijn ook de nodige ethische bezwaren. In dit stadium handelen ze voornamelijk over het feit dat we niet weten wat we creëren: misschien wel een varken met een mensachtig brein? Dat dat weinig ethisch is, staat buiten kijf. “Je wilt geen vermenselijkt dier krijgen.” Maar ook indien die zorg middels vervolgonderzoek wordt weggenomen, blijven er ongetwijfeld ethische bezwaren rondgalmen. Hoe netjes is het bijvoorbeeld om een dier als kweekvat te gebruiken en het enkel en alleen ter wereld te brengen, om het korte tijd later van (vitale) organen te ontdoen?
Met dat alles in gedachten kun je jezelf afvragen of dit dan de beste oplossing is voor het grote donorentekort. Roelen is niet overtuigd. “Het is één van de mogelijke scenario’s, maar het beste? Dat weet ik niet. Het liefste zou je die menselijke stamcellen natuurlijk in vitro – oftewel buiten het lichaam, in een soort kweekvat – uit laten groeien tot nieuwe organen. Maar dat proberen we al jaren.” Met beperkt succes “Het is met name heel lastig gebleken om de 3D-structuur van een orgaan in vitro goed te krijgen. En daar komt bij dat je in een embryo al een bloedvatensysteem hebt en een hart dat bloed en voedingsstoffen rondpompt en afvalstoffen afvoert. In een kweekvat heb je dat allemaal niet. En toch blijft dat eigenlijk de mooiste optie: een soort orgaanfabriek die geen dieren vereist en – maar dat is nóg een stap verder – van patiëntspecifieke stamcellen organen maakt.” Het is – in ieder geval voor complexe organen – nog toekomstmuziek. “Er zijn op deze manier wel al simpele weefsels gemaakt,” vertelt Roelen. “Zo zijn er van stamcellen in vitro bijvoorbeeld een luchtpijp en blaas gemaakt. En ook het hoornvlies kunnen we in vitro maken.” Maar onderzoekers worstelen met de ingewikkeldere onderdelen in ons lijf. Datzelfde geldt eigenlijk voor een andere interessante oplossing voor het donorentekort: regeneratie. “Hierbij herstellen beschadigde of zieke weefsels zichzelf, bijvoorbeeld nadat we in dat weefsel stamcellen hebben aangebracht.” Ook de mogelijkheden van deze aanpak zijn op dit moment beperkt. “Hoornvliesstamcellen worden nu wel eens in beschadigd hoornvlies aangebracht,” weet Roelen. Maar de aanpak biedt nog geen soelaas bij het falen van complexe, vitale organen.
En zo blijven onderzoekers zoeken naar manieren om aan de vraag naar donororganen te voldoen. Het inbrengen van menselijke cellen in een dierlijke embryo is daarbij in dit stadium niet veel meer dan een nieuwe troefkaart. Vervolgonderzoek zal uit moeten wijzen of onderzoekers die daadwerkelijk kunnen verzilveren.