In de jaren zestig hebben wetenschappers de genetische code – de vertaling van DNA naar eiwitten – gekraakt, maar hoe werkt deze code nu precies?
DNA bevat de instructies om eiwitten te maken. Maar het DNA-alfabet bestaat uit vier letters (A, T, G en C), terwijl de taal van de eiwitten twintig letters (zogenaamde aminozuren) telt. Hoe vertaalt de cel DNA-taal naar eiwit-taal? De Russische fysicus George Gamow bekeek het probleem door een wiskundige bril. Hoe kan je vier letters combineren zodat er bij elk van de twintig aminozuren een unieke DNA-code past? Een code op basis van twee DNA-letters werkt niet, want dit levert slechts zestien combinaties op. Te weinig voor de twintig aminozuren. Maar een code met drie DNA-letters behoort wel tot de mogelijkheden. Die code resulteert namelijk in 64 verschillende lettercombinaties, meer dan genoeg voor twintig aminozuren.
Deze oplossing leidde echter tot een volgend probleem. Welke combinatie van drie DNA-letters codeert nu voor welk aminozuur? In 1954 richtte de Amerikaanse bioloog James Watson (samen met Francis Crick ontdekker van de dubbele helixstructuur van DNA) samen met Gamow de RNA Tie Club op om deze genetische code te kraken. Deze club telde twintig leden (één voor elk aminozuur) en vier ereleden. Elk lid kreeg een wollen das met de dubbele helix erop geborduurd. Eén van de leden, de Zuid-Afrikaanse bioloog Sydney Brenner, stelde de term ‘codon’ voor om te verwijzen naar een combinatie van drie DNA-letters. Vierenzestig codons en twintig aminozuren. Het puzzelen kon beginnen.
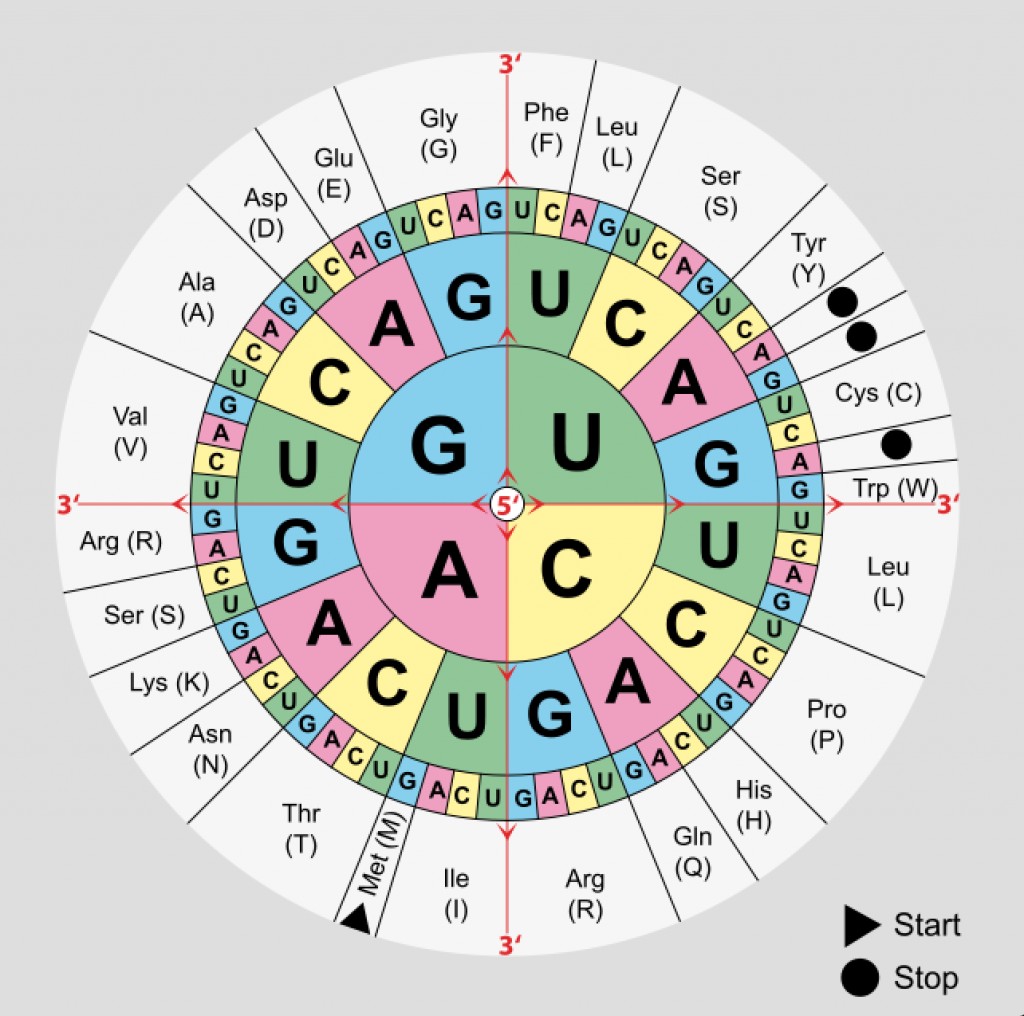
De eerste codons werden ontcijferd met simpele experimenten. Wetenschappers maakten in het lab lange strengen van slechts één DNA-letter. Deze strengen werden vervolgens door een cel vertaald naar een keten van aminozuren. Wanneer men een streng A’s gebruikte, ontstond er een lange keten van het aminozuur lysine. En als men een streng C’s liet vertalen, dan bestond de keten alleen uit het aminozuur proline. De conclusie was glashelder: AAA codeert voor lysine en CCC codeert voor proline. Met verdere experimenten ontcijferden onderzoekers de volledige genetische code. De code bleek zelfs start- en stoptekens te bevatten. Het codon ATG – wat codeert voor methionine – markeert het startpunt van een eiwit, terwijl de codons TAA, TGA en TAG het einde aangeven.
Redundantie
Met vierenzestig codons en twintig aminozuren is het duidelijk dat meerdere codons voor hetzelfde aminozuur coderen. Bijvoorbeeld, AAT en AAC verwijzen beiden naar asparagine. Dit fenomeen, dat bekend staat als de redundantie van de genetische code, biedt de cel enige bescherming tegen mutaties. Een mutatie in een codon kan leiden tot een ander aminozuur of stopteken in de eiwitketen. Stel dat het codon AAA (wat codeert voor lysine) muteert tot TAA (een stopcodon). Door deze mutatie komt er een stopcodon op de verkeerde plek in het eiwit en wordt de productie van dat eiwit vroegtijdig afgebroken met mogelijk negatieve gevolgen voor de cel. Een gedetailleerde blik op de genetische code toont aan dat vele mutaties echter geen schadelijk effect hebben. Neem het aminozuur alanine dat gecodeerd wordt door de codons GCT, GCC, GCA en GCG. Een mutatie op de derde positie van deze codons, bijvoorbeeld van GCT naar GCC, leidt niet tot een verandering in aminozuur, aangezien zowel GCT als GCC verwijzen naar alanine. Na deze mutatie produceert de cel nog steeds identiek hetzelfde eiwit.
Universeel?
Alle levende wezens op deze planeet gebruiken deze genetische code, een belangrijke aanwijzing dat alle organismen afstammen van een gemeenschappelijke voorouder. Toch is de code niet universeel. Door de evolutionaire geschiedenis heen hebben bepaalde organismen de code lichtjes aangepast. Bacteriën van het genus Mycoplasma gebruiken bijvoorbeeld TGA voor tryptofaan hoewel dit codon in de standaardcode een stopcodon is. En bepaalde gisten vertalen CTG naar serine in plaats van leucine. Deze variaties op de genetische code zijn mogelijk een beschermingsmechanisme tegen virussen. Deze ziekteverwekkers maken gebruik van de eiwittenfabrieken in een cel om zich voort te planten. Maar als de genetische code van het virus afwijkt van de code in de cel, kan het virus zich niet voortplanten en wordt de cel dus niet geïnfecteerd.
Eiwitproductie voor dummies
Hoewel een cel vierenzestig codons ter beschikking heeft, worden ze niet allemaal even vaak gebruikt. Dit fenomeen staat in het vakjargon bekend als codon usage bias. En om te begrijpen waar deze kieskeurigheid vandaan komt, moet je weten hoe de eiwitfabriek van de cel functioneert. De productie van eiwitten gebeurt met behulp van ribosomen, complexe structuren van eiwitten en RNA-moleculen, die eruit zien als een hamburgerbroodje zonder groenten of vlees ertussen. Ribosomen ontvangen instructies van het DNA om bepaalde eiwitten te maken. Omdat het DNA-molecuul te groot is om de celkern te verlaten, worden de instructies gekopieerd naar een boodschapper-molecuul, het messenger RNA of mRNA. Je kan dit proces vergelijken met het kopiëren van een recept uit een dik kookboek. Stel dat je het recept voor pasta carbonara nodig hebt (aangezien dit artikel over DNA gaat, lijkt het me logisch om een ‘strengachtig’ gerecht te kiezen). Omdat het internet niet werkt, ga je naar de lokale bibliotheek op zoek naar een Italiaans kookboek. Het boek is veel te dik om mee te sleuren en je vreest dat je tijdens het koken de pagina’s met carbonara-saus zal besmeuren. Daarom schrijf je het recept over op een stukje papier en haast je je terug naar huis om de pasta te bereiden. Er is trouwens een belangrijk verschil tussen de DNA-code en de boodschap van het mRNA. Tijdens het kopiëren vervangt het mRNA de DNA-letter T met de letter U (voor de base uracil). Vandaar dat je in sommige afbeeldingen van de genetische code een U ziet in plaats van een T.
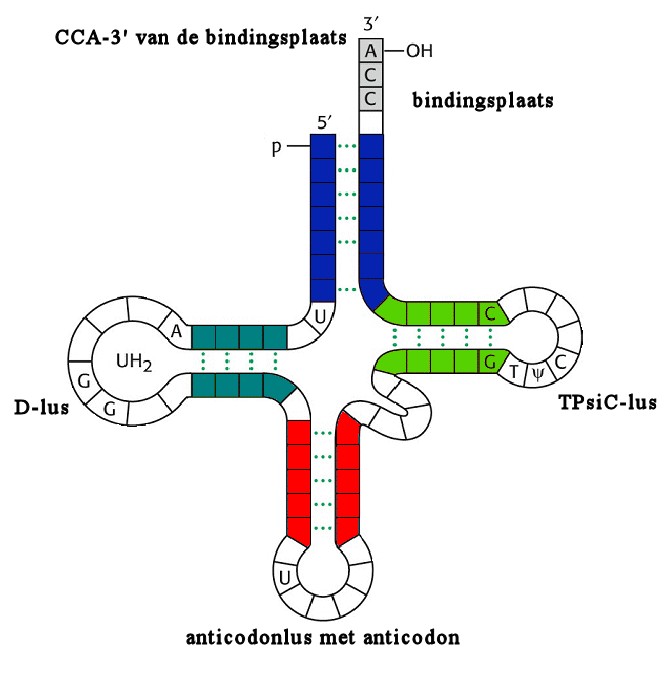
Het mRNA zwemt vervolgens naar de ribosomen, maar de fabriek kan natuurlijk niet werken zonder de juiste grondstoffen. De ‘vrachtwagens’ die de grondstoffen (hier: aminozuren) naar de fabriek brengen zijn de zogenaamde transfer RNAs (tRNA). Deze moleculen hebben de vorm van een klavertje met drie grote lussen. Bovenaan het tRNA-molecuul is een ankerpunt voor de aminozuren en onderaan op één van de lussen vind je een combinatie van drie letters die overeenkomt met de codons op het mRNA. De lettercombinaties op de tRNA-moleculen worden anticodons genoemd aangezien ze de tegenpool vormen van de codons. In de ribosomen bindt het tRNA met het juiste codon op het mRNA en levert zijn aminozuur af. Dit aminozuur wordt aan de groeiende eiwitketen toegevoegd en het tRNA verlaat het ribosoom om zijn volgende lading op te halen. Zo worden eiwitten letterlijk aan de lopende band gemaakt.
tRNAs en codons
Er zijn evenveel soorten tRNAs als codons, namelijk vierenzestig. Elk organisme heeft een bepaald aantal tRNAs per codon ter beschikking. De mens beschikt bijvoorbeeld over 44 tRNAs voor lysine: 24 voor het codon AAG en 20 voor het codon AAA. Er ontbreken ook bepaalde tRNAs in het menselijk genoom, zo zal je geen tRNAs tegenkomen voor GGT (glycine), CGC (arginine) of CAT (histidine). Gelukkig zijn er nog andere tRNAs die deze aminozuren transporteren.
Zou er een verband zijn tussen de beschikbaarheid van specifieke tRNAs en het gebruik van bepaalde codons tijdens de eiwitproductie? Dat is wat sommige wetenschappers vermoeden. Net zoals een fabriek de bestelling van grondstoffen afstemt op de bestellingen van klanten, zo zou de cel zijn diversiteit aan tRNA-moleculen afstemmen op de instructies van het mRNA. Als er veel eiwitten met alanine gemaakt worden, dan is het logisch om veel tRNAs te produceren die alanine naar de ribosomen brengen. In micro-organismen, zoals de bacterie Escherichia coli en de bakkersgist Saccharomyces cerevisae, blijkt er inderdaad een verband te zijn tussen het gebruik van bepaalde codons en de diversiteit aan tRNAs in het genoom. Maar voor andere organismen, waaronder de mens en de fruitvlieg, gaat dit verband niet op. Wetenschappers denken dat hier mutaties een mogelijke rol spelen. Sommige organismen vertonen een ‘voorkeur’ voor specifieke mutaties. Zo hebben bepaalde zoogdieren, zoals het konijn en de spitsmuis, meer mutaties die G’s en C’s produceren waardoor er meer codons met deze letters ontstaan. Het mechanisme achter deze mutatievoorkeur is vooralsnog onbekend. Waarschijnlijk is het overmatig gebruik van bepaalde codons het gevolg van beide processen: de afstemming van codongebruik op de beschikbare tRNAs en een ‘voorkeur’ voor bepaalde mutaties.
Mijn onderzoek
In mijn huidige onderzoeksproject aan het Karolinska Instiutet in Stockholm bestudeer ik de evolutie van tRNAs – de ‘vrachtwagens’ van de eiwitfabriek – bij vogels. In het algemeen hebben vogels 200 à 300 tRNAs, maar enkele soorten hebben er heel wat meer. Zo beschikt de kroeskoppelikaan over bijna 600 tRNAs voor isoleucine en heeft de bandstaarttrogon maar liefst 2750 tRNAs voor valine. Waarom hebben deze vogels zoveel isoleucine en valine nodig? Wat is hier aan de hand? Dat lees je hopelijk binnen enkele maanden op Scientias.nl!
Jente Ottenburghs promoveerde aan de Universiteit Wageningen waar hij onderzoek deed naar de evolutie van ganzen. Na een stage bij de wetenschapsredactie van de Volkskrant werkt hij nu als postdoc aan het Karolinska Institutet in Stockholm (Zweden). Meer weten over Jente? Neem een kijkje op zijn website. Recent kon je in een artikel van de hand van Jente al lezen hoe een genoom in kaart wordt gebracht. Nieuwsgierig? Klik hier! En binnenkort zal ook het artikel hierboven een vervolg krijgen. In dat artikel hoopt Jente de oorsprong van de genetische code uit de doeken te doen.






